
▎药明康德/报导
昨日,2019年诺贝尔生理学或医学奖揭晓获奖名单。William G. Kaelin教授、Peter J. Ratcliffe教授、以及Gregg L. Semenza教授因为对人类以及大多数动物的生计而言,至关重要的氧气感知通路的研讨摘得荣誉。
William G. Kaelin教授(左)、Peter J. Ratcliffe教授(中)、以及Gregg L. Semenza教授(右)(图片来历:参考资料[1])
取得诺贝尔奖的科学研讨不光是基础研讨方面的重要打破,也常常繁殖改动疾病医治的立异疗法。例如上一年诺贝尔生理学或医学奖取得者James Allison教授和与本庶佑教授对免疫检查点CTLA-4和PD-1的研讨,不光直接带来了靶向CTLA-4的抗癌疗法Yervoy和靶向PD-1的抗癌疗法Opdivo,并且催生了免疫检查点按捺剂疗法的出现,彻底改动了癌症医治的格式。
那么本年取得诺贝尔奖的“氧感知通路“又会或许谋福哪些患者呢?今日药明康德内容团队将与读者探求这一信号通路带来的立异疗法。
医治贫血的立异疗法
氧感知通路的中心部分为HIF-1蛋白,它可以激活动物细胞中多个对缺氧环境发生反响的基因,包含VEGF,促红细胞生成素(erythropoietin,EPO)等等。这些基因表达的蛋白可以影响血红细胞的生成,血管增生等生理进程,协助机体取得更多的氧气。
生物体感知氧气的通路示意图(图片来历:参考资料[2],Credit:Cassio Lynm)
靶向这一通路的立异疗法现已在医治贫血患者方面体现出了杰出的作用。贫血患者身体中血红细胞水平缺乏,无法将满足的氧气运送到身体各个部位。
在医治贫血方面,安进公司(Amgen)出产的重组人促红细胞生成素(EPO)是一款现已有30年前史的有用疗法。而EPO也是氧感知通路的下流靶点,遭到HIF-1蛋白的调控。近年来,多家生物医药公司现已开宣布立异疗法,经过进步HIF-1蛋白的水平来调理人体对缺氧状况的反响。因为HIF-1蛋白可以调控与处理缺氧状况相关的多个生理进程,包含血红细胞的生成和铁元素的运送等等,靶向HIF-1蛋白的调控剂有望取得比EPO更好的医治作用。
低氧诱导因子脯氨酰羟化酶按捺剂(HIF-PHI)作用机理(图片来历:参考资料[3])
现在至少有6款低氧诱导因子脯氨酰羟化酶按捺剂(HIF-PHI)处于临床开发阶段。HIF脯氨酰羟化酶经过对HIF的润饰,导致HIF被蛋白酶体降解,然后下降机体内的HIF水平。它是细胞在富氧环境下下降HIF水平的重要调控机制。HIF-PHI经过按捺HIF脯氨酰羟化酶的作用,进步HIF-1的水平,然后起到缓解贫血的作用。
由珐博进(Fibrogen)、阿斯利康(AstraZeneca)和安斯泰来(Astellas)联合开发的“first-in-class“HIF-PHI罗沙司他(roxadustat)现已在上一年12月初次在我国获批上市,医治正在承受透析医治的患者因缓慢肾病(CKD)引起的贫血。它在本年不光又在我国获批扩展适应症,医治无需承受透析医治的肾性贫血患者,还在日本获批上市。
此外,拜耳(Bayer)的molidustat和葛兰素史克(GSK)的daprodustat也都现已在日本递交了新药请求,而Akebia Therapeutics公司的vadadustat和Zydus Cadila公司的desidustat处于3期临床开发阶段。
部分HIF-PHI分子结构式(图片来历:Meodipt [Public domain])
医治癌症的立异疗法
在多种癌症中,因为癌细胞的敏捷增殖,通常会形成在肿瘤邻近的部分供氧缺乏,因而癌细胞常常会进步HIF-1α蛋白的表达,影响机体的血管增生,为肿瘤供给更多氧气和营养。此外,不同基因骤变也会形成HIF-1α的表达添加,包含致癌基因的功用取得性骤变(例如ERBB2),以及抑癌基因的功用损失性骤变(例如VHL和PTEN)。HIF-1调控的基因与肿瘤的代谢,增殖、生计和搬运,以及肿瘤血管增生休戚相关。因而,按捺HIF-1蛋白和其相关蛋白(HIF-2α)的功用也成了抗癌药物研制的重要方向之一。
HIF-1调理的与癌症相关的部分基因(图片来历:参考资料[4])
但是,现在还没有一款取得同意的HIF按捺剂。这一研制方向面对的首要应战是发现具有特异性的HIF按捺剂。另一个或许下降HIF按捺剂作用的原因是HIF蛋白宗族中不同成员的功用可以互补。例如,研讨标明假如敲低HIF-1α的表达会导致HIF-2α的表达补偿性升高。这意味着要想按捺癌症的成长,或许需求一起靶向HIF-1α和HIF-2α。因为HIF信号通路在影响血红细胞增生方面的重要功用,HIF按捺剂的一个常见副作用是贫血,这也会影响它们医治癌症患者的安全性。
现在,特异性靶向HIF信号通路的抗癌疗法包含Peleton Therapeutics公司开发的“first-in-class“HIF-2α按捺剂PT2977。它可以特异性地与HIF-2α结合,按捺HIF-2α与HIF-1β的结合。现在它在2期临床实验中用于医治与VHL相关的晚期肾细胞癌患者。默沙东(MSD)公司在本年5月斥资22亿美元收买了Peleton公司。
另一款靶向HIF信号通路的抗癌疗法是罗氏(Roche)公司靶向HIF-1α的反义寡核苷酸疗法RO7070179。这款反义寡核苷酸疗法现在在1b期临床实验中医治肝细胞癌患者。实验结果标明,RO7070179可以在疾病安稳和取得部分缓解的肝细胞癌患者中下降HIF-1α的mRNA水平。
结语
除了医治贫血和癌症以外,HIF-1α安稳剂还被用于医治炎症性肠病。学术研讨标明,HIF-2α还或许成为医治非酒精性脂肪性肝炎的新靶点。
本文题图:Photo by Adam Baker, 'Nobel Prize Medal in Chemistry' CC BY 4.0 (https:///photos/atbaker/8459286843), via Flickr
参考资料:
[1] The Nobel Prize in Physiology or Medicine 2019, Retrieved October 7, 2019, from https:///pipeline/pipeline-overview/
[6] FibroGen, Inc. Corporate Presentation. Retrieved October 7, 2019, from https://fibrogen.gcs-web.com/static-files/c82c7b58-d8d5-4567-93b6-0e85ac6b2105
[7] Akebia Therapeutics. Retrieved October 7, 2019, from https://akebia.com/research-and-development/vadadustat.aspx
[8] Yu et al., (2017). Development of Inhibitors Targeting Hypoxia-Inducible Factor 1 and 2 for Cancer Therapy. Yonsei Medical Journal, Doi: 10.3349/ymj.2017.58.3.489
[9] Xie et al., (2017). Activation of intestinal hypoxia-inducible factor 2α during obesity contributes to hepatic steatosis. Nature Medicine, https://doi.org/10.1038/nm.4412
[10] Merck to Acquire Peloton Therapeutics, Bolstering oncology Pipeline. Retrieved October 7, 2019, from https://investors.merck.com/news/press-release-details/2019/Merck-to-Acquire-Peloton-Therapeutics-Bolstering-Oncology-Pipeline/default.aspx
[11] GSK submits first regulatory application for daprodustat in Japan for patients with renal anaemia due to chronic kidney disease. Retrieved October 7, 2019, from https:///en-gb/media/press-releases/gsk-submits-first-regulatory-application-for-daprodustat-in-japan-for-patients-with-renal-anaemia-due-to-chronic-kidney-disease/
[12] Wu et al., (2019). evaluation of a locked nucleic acid form of antisense oligo targeting HIF-1α in advanced hepatocellular carcinoma. World J Clinical Oncology, doi: 10.5306/wjco.v10.i3.149
版权阐明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或组织未经授权以任何方式转载至其他渠道。转载授权请在「药明康德」微信大众号回复“转载”,获取转载须知。

 沃尔沃汽车“移动的体育博物馆”焕新发车 以车为展,助力体育运动全民
沃尔沃汽车“移动的体育博物馆”焕新发车 以车为展,助力体育运动全民 共筑社会“安全感”|沃尔沃汽车鼎力支持上海市“医苑新星”结业仪式
共筑社会“安全感”|沃尔沃汽车鼎力支持上海市“医苑新星”结业仪式 重庆丰益中医肛肠医院看病贵不贵?收费透明,看病不贵
重庆丰益中医肛肠医院看病贵不贵?收费透明,看病不贵 校园直击!紫竹蜂胶口腔膜治愈风潮燃动福州!
校园直击!紫竹蜂胶口腔膜治愈风潮燃动福州! 万众瞩目:络病大会召开 微血管病变防治开辟新局面
万众瞩目:络病大会召开 微血管病变防治开辟新局面 毓婷x学院奖云课堂完美收官|“毓”青春同行,创意步履不“婷”
毓婷x学院奖云课堂完美收官|“毓”青春同行,创意步履不“婷”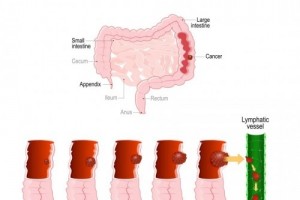 发现就是中晚期的结直肠癌,其实有办法可以避免!
发现就是中晚期的结直肠癌,其实有办法可以避免! “毓”见别YOUNG青春——毓婷携手学院奖2022再启新程
“毓”见别YOUNG青春——毓婷携手学院奖2022再启新程